첨생법 개정안 국회 본회의 통과…내년부터 본격 시행
모든 질환 임상 연구 가능·첨단재생의료 치료 가능해져
GC셀 등 첨단재생의료업계 기대감↑…협회 “적극 지원”
내년부터 국내에서도 중대·희귀·난치질환자들이 세포유전자 치료 등 첨단재생의료 혜택을 받을 수 있게 된다.
첨단재생의료는 사람의 신체 구조나 기능을 인체 세포 등을 이용해 대체하는 등 질병을 치료(완치)하는 것을 의미한다. 대표적으로 세포·유전자치료, 이종장기이식 등이 있다.
6일 제약바이오업계에 따르면 지난 1일 첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률(이하 첨생법)이 국회 본회의를 통과했다.
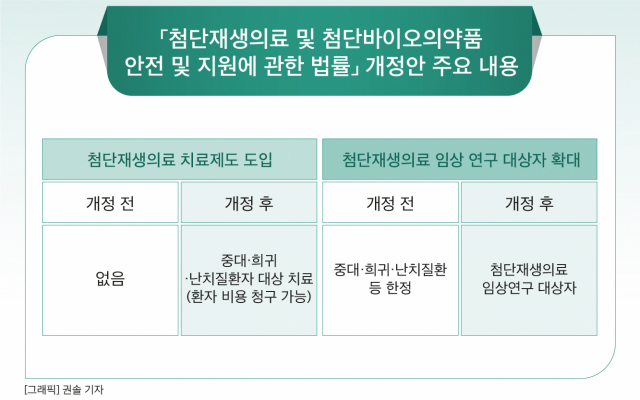
개정안은 중대·희귀·난치질환자의 치료기회 확대와 관련 연구·산업 발전의 기반을 강화하기 위해 ‘첨단재생의료’를 도입하고, 임상연구 대상범위를 확대하는 것을 골자로 하고 있다. 개정안은 공포 후 1년 경과한 날부터 본격 시행된다.
첨단재생의료 치료 대상자는 중대·희귀·난치질환자다. 그동안 이들은 첨단재생의료 치료를 받고 싶어도 해당 법이 없어 치료를 받을 수 없었다. 이에 일부 환자들은 관절염·면역치료 등을 목적으로 줄기세포 치료를 받기 위해 일본 원정을 떠나기도 했다. 하지만 첨생법 개정안이 시행되면 임상에 참여한 환자가 아니어도 중대·희귀·난치 질환자가 희망하는 경우 법이 정한 기준에 따라 세포·유전자 치료를 받을 수 있다.
예를 들어 교모세포종과 같은 대체치료제가 없는 악성 뇌종양 환자들의 경우 정식 허가가 나기 전이라도 임상을 통해 유효성과 안전성이 확보된 첨단재생의료 치료제가 있다면 사용할 수 있는 기회가 생긴다. 다만, 복지부는 치료 안정성 확보를 위해 사전에 지정된 기관이 제출한 치료계획을 심의해 실시 여부를 결정한다.
또, 첨단재생의료 임상연구 대상자도 확대했다. 그동안은 사전 승인을 받은 중대·희귀·난치질환만 연구대상이었지만 앞으로는 질환을 갖고 있는 환자가 임상연구의 대상이 될 수 있다.
첨생법은 지난 2020년 8월부터 시행됐지만 내용이 매우 제한적이라 개정을 요구하는 업계의 목소리가 높았다. 첨단재생의료 임상연구가 제한적으로 이뤄지고, 첨단재생의료 치료가 금지돼 환자의 치료받을 권리가 침해되는 등 첨단재생의료 산업 발전이 저해된다는 이유에서다.
업계에서는 개정안 국회 통과가 국내 세포·유전자 치료제 시장에 긍정적인 영향을 줄 것으로 기대하고 있다.
제임스 박 GC셀 대표는 “첨생법 개정안 통과를 계기로 중증 희귀난치성 질환의 치료 기회가 확대됨에 따라 더 많은 환자들에게 치료 기회를 제공할 수 있게 됐다”면서 “앞으로 세포·유전자 치료제 연구개발에 더욱 탄력이 붙을 것으로 기대된다”고 말했다.
GC셀은 현재 항암면역세포치료제인 ‘이뮨셀엘씨주’를 생산·판매하고 있다. 회사는 자사 파이프라인 임상·상업화에 더욱 속도를 낸다는 계획이다.
첨단재생의료산업협회(CARM)도 기대감을 드러냈다. 최근 CARM 회장에 선임된 이득주 녹십자홀딩스 상임고문은 “첨단재생바이오법에 대한 일부 개정안이 지난 2월1일 국회를 통과해 세포치료, 유전자치료 등 첨단재생의료 시장에서 많은 변화가 예상되고 있다”며 “국가 의료 발전과 국민 건강 증진을 위해 정책당국과 규제 개선 및 정책지원 효율화를 위해 적극 지원 하겠다”고 말했다.
[CEO스코어데일리 / 조희연 기자 / chy@ceoscore.co.kr]



![[현장을 가다] 아모레뷰티파크에서 탄생 100주년 서성환 선대회장의 '동백나무 정신'을 만나다](https://www.ceoscoredaily.com/photos/2024/03/22/2024032213414139276_m.jpg)
![[현장을 가다] “‘아리아’가 나를 살렸어”…SKT ‘AI 스피커’, 어르신 말동무 이자 ‘보디가드’로 활약](https://www.ceoscoredaily.com/photos/2024/04/01/2024040109491192497_m.jpg)
![[현장을 가다] ‘자동차 메카’에서 ‘전기차 허브’로…현대차 울산공장 가보니](https://www.ceoscoredaily.com/photos/2024/03/22/2024032216190656760_m.jpg)

![[그래픽] 롯데GRS 실적 추이](https://www.ceoscoredaily.com/photos/2024/04/26/2024042609264395390_m.jpg)
























































































![[24-03호]_500대기업 R&D 투자 현황](https://www.ceoscoredaily.com/photos/2024/04/17/2024041718513086340_m.jpg)

![[이달의 주식부호] 홍라희 여사 2위 탈환…곽동신 한미반도체 부회장 6위로 2계단↑](https://www.ceoscoredaily.com/photos/2024/04/03/2024040314314813956_m.jpg)



![[그래픽] 그레이트 컴퍼니 우수기업 리스트](https://www.ceoscoredaily.com/photos/2023/08/24/2023082410452781615_m.jpg)



댓글
[ 300자 이내 / 현재: 0자 ]
현재 총 0개의 댓글이 있습니다.